Sono state recentemente pubblicate le linee guida dell’European Society of Medical Oncology (ESMO) sulla gestione del tromboembolismo venoso (TEV) nel paziente affetto da cancro (1).
Il documento europeo si propone di fornire indicazioni e raccomandazioni usando uno stile semplice, facilmente fruibile, nel tentativo di implementare il più possibile l’uso delle linee guida fra i medici oncologi. Infatti, nonostante molte linee guida sulla gestione del TEV in oncologia siano state prodotte dalle più importanti Società scientifiche (2,3,4,5), tuttavia la loro applicazione, soprattutto per quanto riguarda la profilassi del TEV, è ancora scarsa.
Il miglioramento delle cure, a cui abbiamo assistito negli ultimi anni, ha paradossalmente condotto ad un aumento di tre volte dei casi di TEV nei pazienti neoplastici, sia per la prolungata sopravvivenza e la maggiore efficienza degli strumenti diagnostici (con il frequente riscontro di trombosi asintomatiche) che per l’aumentato rischio trombotico legato ad alcune nuove ed efficaci terapie antineoplastiche.
Ecco allora la stringente necessità di individuare non solo la cura più efficace e sicura per questo tipo di pazienti ma anche la migliore prevenzione.
Nel documento ESMO viene sottolineata per la prima volta la necessità di informare il paziente oncologico sui fattori di rischio, i segni ed i sintomi con cui si può presentare il tromboembolismo venoso (per un accesso tempestivo ed efficace alle cure) e sui corretti stili di vita.
Tuttavia, la prevenzione passa anche attraverso la somministrazione, in casi selezionati, di una adeguata profilassi farmacologica, che non è indicata in tutti i pazienti, ma solo in quelli in cui l’alto rischio trombotico sovrasta l’evidente rischio emorragico. Ma come individuare chi può trarre il massimo beneficio dalla profilassi con farmaci anticoagulanti?
Il problema è complesso poiché, in particolare nei pazienti ambulatoriali che si sottopongono a terapie antitumorali (chemioterapia, immunoterapia, ormonoterapia, etc), il rischio trombotico è molto variabile, a seconda dello stadio, del tipo di tumore, delle condizioni generali del paziente, del tipo di terapie e di molti altri fattori. Individuare uno “score” che tenga conto di tutti queste variabili è una sfida che ha impegnato i ricercatori nelle ultime due decadi portando alla validazione nel 2008 dello score di Khorana (6), che è stato utilizzato per individuare i pazienti da sottoporre a tromboprofilassi nei trials clinici randomizzati AVERT e CASSINI (7,8). Rispetto alle linee guida precedenti, il documento ESMO include altri due “score” per la valutazione del rischio, recentemente validati esternamente, il COMPASS ed il VIENNA-CAT score (quest’ultimo include solo il tipo di tumore ed il D-dimero). Tuttavia, gli autori sottolineano come la ricerca di uno strumento che riesca ad individuare nel modo migliore i pazienti da sottoporre a tromboprofilassi farmacologica sia ancora in corso.
Secondo le indicazioni del panel di esperti (1), nei pazienti ambulatoriali che iniziano una terapia antineoplastica sistemica ed hanno un alto rischio trombotico (identificato con i suddetti score) possono essere presi in considerazione per la tromboprofilassi primaria (per un massimo di 6 mesi) apixaban, rivaroxaban o eparina a basso peso molecolare (EBPM) [I, B]. Tuttavia, nonostante un analogo documento AIOM (Associazione Italiana di Oncologia Medica) si esprima negli stessi termini, in Italia i DOAC non sono ancora autorizzati per questa indicazione.
Inoltre, le linee guida ESMO danno indicazioni specifiche per il paziente con cancro del pancreas in chemioterapia, nel quale dosi più alte di EBPM rispetto a quelle standard sono raccomandate per la profilassi, per un massimo di 3 mesi [II, C]. Infine, il documento include le raccomandazioni sulla tromboprofilassi nel paziente con mieloma multiplo.
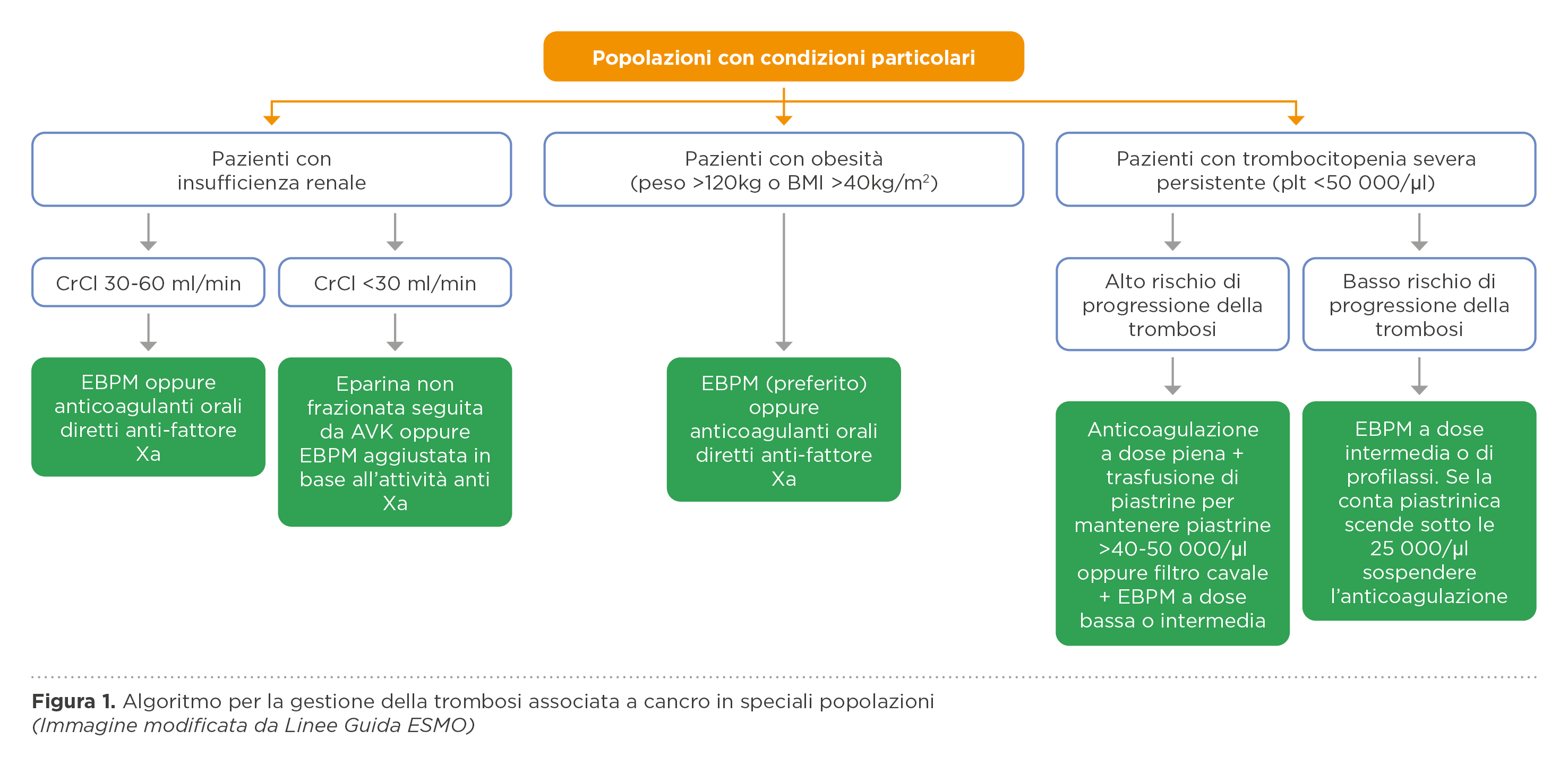
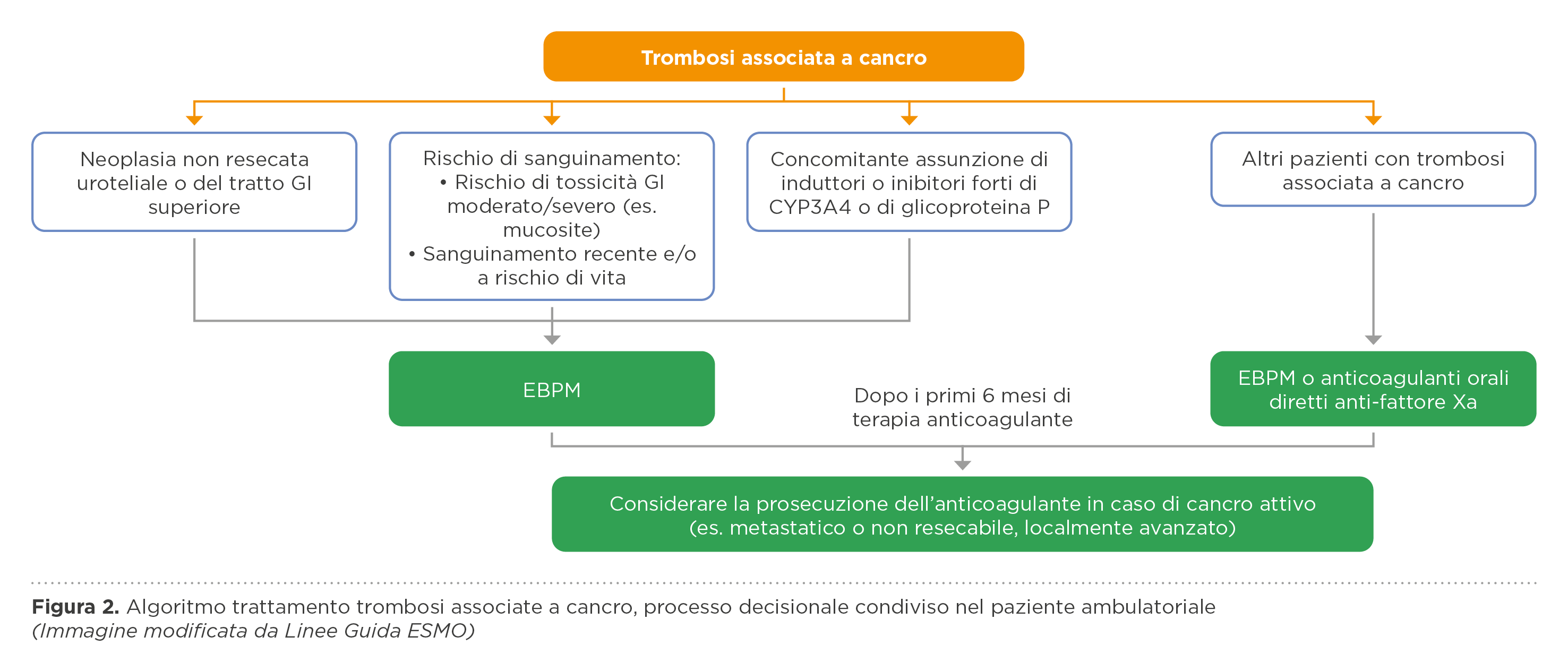
Per quanto riguarda la terapia della trombosi venosa profonda o dell’embolia polmonare conclamate, la terapia di elezione nel paziente oncologico è stata per quasi due decadi l’EBPM, dopo i grandi trials degli anni duemila, che ne avevano dimostrato la superiorità rispetto al warfarin. Tuttavia, già dal 2019 le linee guida internazionali (2,3,4,5) hanno recepito i risultati degli studi randomizzati controllati che hanno dimostrato l’efficacia e la sicurezza dei DOAC per questa indicazione clinica, raccomandandone l’utilizzo in alternativa all’EBPM. Naturalmente è necessario tenere conto delle potenziali interferenze farmacologiche (ad esempio la concomitante assunzione di inibitori o attivatori del citocromo p450 2B3A e della glicoproteina P), e dell’elevato rischio emorragico associato con le neoplasie del tratto gastrointestinale o genitourinario. Le raccomandazioni ESMO includono sia i DOAC che EBPM. Inoltre, il documento ESMO ha il pregio di fornire indicazioni pratiche su come comportarsi in casi particolari, come i pazienti con piastrinopenia severa, quelli con insufficienza renale e quelli con alto peso corporeo, trattati solo marginalmente dalle linee guida precedenti (figura 1 e 2). Infine, esso include anche la profilassi e la terapia del TEV associato all’uso di cateteri venosi centrali o periferici, spesso oggetto di documenti e linee guida separate. Cosa importante, gli autori tengono ripetutamente a sottolineare come ogni scelta terapeutica vada discussa e condivisa con il paziente, tenendo conto delle sue preferenze, necessità ed orientamenti, nell’ottica di un miglioramento, quanto più possibile, della qualità di vita.
“L’intento di queste linee guida è di voler essere chiare e di semplice consultazione, attraverso schemi ed algoritmi, e di estendersi dalla diagnosi del TEV fino a tutte le principali condizioni in cui è necessario prendere decisioni sulla più appropriata profilassi e terapia del TEV in questi pazienti, che sono ad alto rischio”- ha spiegato la Prof.ssa Anna Falanga, primo autore del documento -“Le linee guida ESMO hanno un’ampia diffusione tra gli oncologi europei e nei Paesi dell’Est fino al Medio Oriente e tutto il bacino del Mediterraneo. Il nostro auspicio è che vengano adottate largamente e che vi sia un miglioramento nella conoscenza di queste frequenti complicanze e della loro gestione nella popolazione oncologica”-ha concluso Falanga.
- Falanga A, Ay C, Di Nisio M, et al. Venous thromboembolism in cancer patients: ESMO Clinical Practice Guideline†[published online ahead of print, 2023 Jan 3]. Ann Oncol. 2023;S0923-7534(22)04786-X. doi:10.1016/j.annonc.2022.12.014
- Farge D, Frere C, Connors JM, Ay C, Khorana AA, Munoz A, et al. International clinical practice guidelines for the treatment and prophylaxis of venous thromboembolism in patients with cancer. Lancet Oncol 2019;20:e566–81. https://doi.org/10.1016/S1470-2045(19)30336-5. 2019.
- Key NS, Khorana AA, Kuderer NM, Bohlke K, Lee AYY, Arcelus JI, et al. Venous thromboembolism prophylaxis and treatment in patients with cancer: ASCO clinical practice guideline update. J Clin Oncol 2020;38:496–520. https://doi.org/10.1200/JCO.19.01461.
- Lyman GH, Carrier M, Ay C, Di Nisio M, Hicks LK, Khorana AA, et al. American Society of Hematology 2021 guidelines for management of venous thromboembolism: prevention and treatment in patients with cancer. Blood Adv 2021;5:927–74. https://doi.org/10.1182/bloodadvances.2020003442.
- NCCN guideline on cancer-associated venous thromboembolic disease. Version 1 [n.d] Oncol 2022. Available at: . [Accessed March 2022].
- Khorana AA, Kuderer NM, Culakova E, Lyman GH, Francis CW. Development and validation of a predictive model for chemotherapy-associated thrombosis. Blood. 2008;111(10):4902-4907. doi:10.1182/blood-2007-10-116327
- Carrier M, Abou-Nassar K, Mallick R et al. Apixaban to Prevent Venous Thromboembolism in Patients with Cancer. N Engl J Med 2019; 380 (8): 711- 719.
- Khorana AA, Soff GA, Kakkar AK et al. Rivaroxaban for Thromboprophylaxis in High-Risk Ambulatory Patients with Cancer. N Engl J Med 2019; 380 (8): 720-728