I nuovi criteri classificativi, così come i precedenti del 2006 (2), non sono criteri diagnostici (anche se spesso utilizzati a tale scopo), ma hanno l’obiettivo di individuare pazienti con caratteristiche omogenee che possano essere inclusi negli studi clinici sulla sindrome da anticorpi antifosfolipidi, indispensabili dati i molti quesiti diagnostici e terapeutici ancora aperti.
Come in precedenza, è necessaria la presenza di almeno un criterio clinico ed uno di laboratorio per poter classificare il paziente come affetto da APS, ma viene introdotto un sistema a “punteggio” per cui sono richiesti almeno tre punti per il criterio clinico e tre punti per quello di laboratorio. Inoltre, viene ridotto a tre anni il tempo che può intercorrere tra la manifestazione clinica e la positività dei test (Figura 1).
Nell’indicare i nuovi criteri classificativi i ricercatori hanno evidenziato e specificato problematiche cliniche meritevoli di attenzione perché potrebbero rispecchiare una condizione di APS.
Infatti, se come sempre l’insorgenza di una trombosi macro vascolare venosa (embolia polmonare o trombosi venosa profonda) o arteriosa (infarto o ictus), in particolare se occorsa in assenza di importanti fattori di rischio, deve far sorgere il sospetto di una APS, gli esperti evidenziano anche possibili presentazioni microvascolari più subdole, quali quelle cutanee (come la livedo racemosa e la vasculopatia livedoide), renali (nefropatia acuta e cronica con trombosi microvascolari glomerulari), polmonari (emorragia polmonare), miocardiche (danno miocardico a coronarie indenni) e surrenaliche (emorragia surrenalica).
Da notare come, a differenza delle precedenti indicazioni, in presenza di ischemia o infarto parenchimale documentato all’imaging non sia più necessario visualizzare il trombo. Inoltre, sorprendentemente, vengono incluse a fini classificativi le occlusioni venose retiniche e le trombosi arteriose retiniche.
Notevole rilievo viene dato anche al danno valvolare cardiaco: il riscontro non solo di vegetazioni valvolari non infettive ma anche, nonostante la minore specificità, di ispessimenti valvolari cardiaci con determinate caratteristiche potrebbe essere suggestivo di APS.
Importanti cambiamenti riguardano i criteri classificativi per la patologia ostetrica. In particolare viene messo in evidenza come il verificarsi di pre-eclampsia o insufficienza placentare con caratteristiche di gravità , debbano far sorgere il sospetto di APS a prescindere dal verificarsi o meno di morte fetale; inoltre, il criterio della poliabortività (≥ 3 eventi), è stato esteso ad includere sia gli aborti pre-fetali(< 10 settimane) che fetali precoci (tra le 10 e le 15 settimane).
Per quanto riguarda i criteri di laboratorio, vengono (finalmente) “derubricati” gli anticorpi di classe IgM anti cardiolipina (aCL) o antiβ2glicoproteinaI (aβ2GPI), poiché ormai ampliamente documentata la minore associazione con eventi clinici, mentre viene attribuita un’importanza piuttosto elevata (forse troppo) alla singola positività (persistente) di grado moderato (40-79U) per gli anticorpi anti aCL e\oaβ2GPI di classe IgG. Il massimo “punteggio” è correttamente attribuito alla concomitante presenza di anticorpi di classe IgG anti aCL e aβ2GP. Da notare come anche una positività “one time” del test per il lupus anticoagulant (LAC) viene considerata meritevole di attenzione.
Tuttavia, va ricordato che a fini clinici diagnostici e terapeutici (e non “classificativi” o di ricerca), ciò che conta è soprattutto il profilo anticorpale, ovvero la presenza di multiple piuttosto che singole positività, il loro titolo, e la persistenza delle positività a misurazioni ripetute (3). Inoltre, test addizionali, come gli anticorpi antifosfatidilserina/protrombina (aPS/PT) possono essere importanti nei casi dubbi e potrebbero aiutarci in futuro a capire qual è il rischio effettivo di questi pazienti (4).
Per di più, la necessità di standardizzare i dosaggi anticorpali, tramite lo sviluppo di materiale di riferimento certificato, ed armonizzare i test tra i vari laboratori, garantendo uniformità nei risultati, rimangono problemi aperti.
Da ultimo, va evidenziato che i criteri classificativi si basano solo su test ELISA per la determinazione del titolo anticorpale aCL e\o aβ2GPI. La scelta di valori limite fissi (40 GPL o MPL e 80 GPL o MPL non è pienamente supportata dalla letteratura esistente (5). I vari test ELISA disponibili non sono comparabili: i nostri dati dimostrano che si possono ottenere risultati diversi con lo stesso campione a seconda della scelta del metodo ELISA, mettendo in dubbio la difendibilità di un cut-off “fisso”(6). Sembra invece più prudente utilizzare il 99° percentile, come precedentemente raccomandato dall’ISTH, che può variare a seconda del fornitore ELISA e dovrebbe essere determinato localmente.
Infine, molti laboratori non usano più sistemi ELISA per la determinazione dei test immunologici ma solo test automatizzati. Per capire l’entità del titolo anticorpale con questi nuovi metodi ogni laboratorio dovrebbe correlare il titolo con quello ottenuto con lo specifico test ELISA usato nel laboratorio. Ciò serve per valutare l’andamento del titolo anticorpale nel tempo rispetto a quello ottenuto in precedenza mediante ELISA.
A cura di Stefania Cavazza e Vittorio Pengo
Figura 1
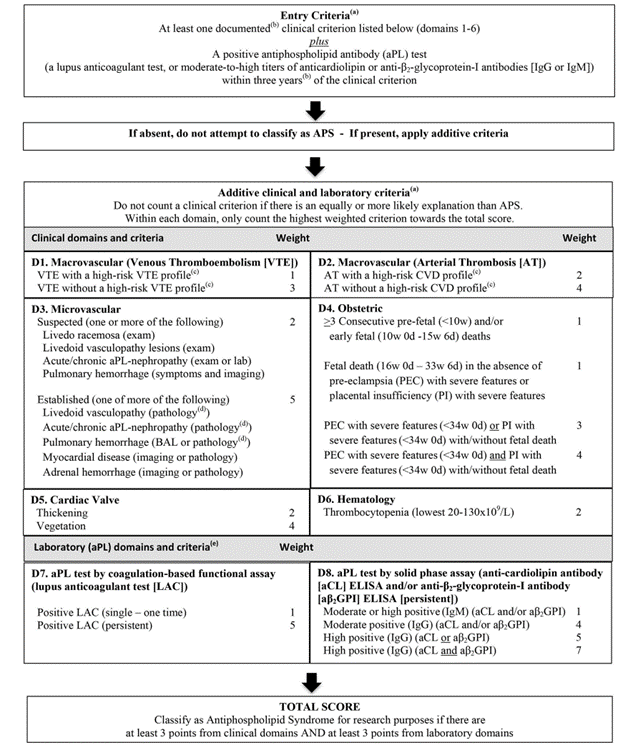
Da Barbhaiya M, et al. Ann Rheum Dis 2023;82:1258–1270.
Bibliografia
- Barbhaiya M, et al; ACR/EULAR APS Classification Criteria Collaborators. 2023 ACR/EULAR antiphospholipid syndrome classification criteria. Ann Rheum Dis. 2023 Oct;82(10):1258-1270. doi: 10.1136/ard-2023-224609. Epub 2023 Aug 28. PMID: 37640450.a
- Miyakis S, et al. International consensus statement on an update of the classification criteria for definite antiphospholipid syndrome (APS). J Thromb Haemost. 2006 Feb;4(2):295-306. doi: 10.1111/j.1538-7836.2006.01753.x. PMID: 16420554.
- Tektonidou MG,et al. EULAR recommendations for the management of antiphospholipid syndrome in adults. Ann Rheum Dis. 2019 Oct;78(10):1296-1304. doi: 10.1136/annrheumdis-2019-215213. Epub 2019 May 15. PMID: 31092409.
- Vandevelde A, et al. Added value of antiphosphatidylserine/prothrombin antibodies in the workup of obstetric antiphospholipid syndrome: communication from the ISTH SSC Subcommittee on Lupus Anticoagulant/Antiphospholipid Antibodies. J Thromb Haemost. 2023 Jul;21(7):1981-1994. doi: 10.1016/j.jtha.2023.04.001. Epub 2023 Apr 13. PMID: 37061133.
- Huisman A, et al. Antiphospholipid antibody solid phase-based assays: problems and proposed solutions for the 2023 ACR/EULAR classification criteria for antiphospholipid syndrome. J Thromb Haemost. 2023 Dec 23:S1538-7836(23)00917-0. doi: 10.1016/j.jtha.2023.12.019. Epub ahead of print. PMID: 38142843.
- Pengo V, Biasiolo A, Bison E, Chantarangkul V, Tripodi A; Italian Federation of Anticoagulation Clinics (FCSA). Antiphospholipid antibody ELISAs: survey on the performance of clinical laboratories assessed by using lyophilized affinity-purified IgG with anticardiolipin and anti-beta2-Glycoprotein I activity. Thromb Res. 2007;120(1):127-33.