Le eparine a basso peso molecolare sono attualmente gli anticoagulanti più comunemente usati nei bambini e neonati.
Tuttavia, dal momento che le complicanze trombotiche raramente si verificano al di fuori dei grandi ospedali pediatrici, i medici spesso incontrano alcuni problemi pratici nella gestione di questi trattamenti se uno specialista di trombosi pediatrico non è disponibile.
Il farmaco di scelta è l’enoxaparina, grazie al suo favorevole rapporto antiFXa/antiFIIA, la lunga emivita e la disponibilità di dati di farmacocinetica e farmacodinamica.
Il trattamento della trombosi acuta deve essere iniziato con due iniezioni quotidiane, ma quando la compliance è un problema una singola somministrazione giornaliera può essere usata per la profilassi secondaria monitorando attentamente l’inibizione dle FXa post 24 h.
Un dispositivo sottocutaneo può essere uno strumento utile e un anestetico locale può essere efficace nel controllo del dolore senza influenzare livelli di anti-FXa.
In neonato e bambini, dove sono spesso necessari mini dosi, lo spazio morto di siringhe ed aghi potrebbe rappresentare un problema e quindi l’uso di siringhe da insulina senza spazio morto è consigliabile, mentre una diluizione del farmaco è utile con altre siringhe. L’utilizzo di un dispositivo sottocutaneo come Insuflon® migliora la compliance ma rende necessaria la diluizione per le dosi minori.
Introduzione
Il problema del tromboembolismo venoso (TEV) infantile è sempre più diffuso. Le linee guida per la terapia antitrombotica dell’American College of Chest Physicians sono disponibili sia per i neonati sia per i bambini da più di dodici anni. Dopo sei edizioni, le raccomandazioni per la terapia anticoagulante sono aumentate da venticinque a più di cento. Gli antagonisti della vitamina K (AVK) sono sempre meno usati perché riservati principalmente al trattamento a lungo termine dei bambini sottoposti a chirurgia cardiaca, e mentre i nuovi anticoagulanti orali sono ancora oggetti di sperimentazione in ambito pediatrico, le eparine a basso peso molecolare (EBPM) sono attualmente gli anticoagulanti più comunemente utilizzati.
La gestione del TEV nei bambini e neonati è più complessa che negli adulti, quindi dovrebbe sempre essere consultato un ematologo pediatra o un esperto di trombosi pediatrica. Tuttavia, mentre il TEV nei bambini e neonati può essere comune in centri di cura terziari, esso è raramente diagnosticato fuori dai grandi ospedali per bambini, e le unità emostasi e trombosi non sono una dotazione standard in ospedali pediatrici; pertanto i medici che devono iniziare la terapia con EBPM in un neonato o in un bambino possono incontrare alcuni problemi pratici che non sono risolti facilmente o rapidamente con la letteratura disponibile.
Questo lavoro deriva dalla nostra pratica clinica in un grande ospedale pediatrico terziario unita a una revisione non sistematica della letteratura disponibile, con particolare attenzione alle recenti linee guida internazionali e le raccomandazioni degli esperti. In questo lavoro, offriremo soluzioni facili e veloci ai problemi più frequenti che i medici, farmacisti e infermieri incontrano in situazioni del genere.
Scelta del farmaco
Sulla base della letteratura disponibile, l’enoxaparina è l’EBPM più utilizzata nei neonati e nei bambini. Inoltre, ci sono alcune altre ragioni i per preferire enoxaparina:
- Enoxaparina è, fra le EBPM, il composto con il miglior rapporto di inibizione fattore Xa / fattore IIa (FXa / FIIA).
- Enoxaparina ha l’emivita più lunga. Questa caratteristica implica la capacità di fornire un effetto anticoagulante prolungato ancora presente ventiquattro ore dopo la somministrazione; in una coorte di 126 bambini che hanno ricevuto enoxaparina una o due volte il giorno, un livello minimo sopra il range desiderato per la profilassi di 0,1 IU ml di attività anti-FXa è stato ottenuto in 53,2% dei pazienti in monodose.
- La disponibilità di dati pediatrici di farmacocinetica e farmacodinamica ottenuti per enoxaparina negli ultimi venti anni fa questo composto preferibile alle altre EBPM.
Tuttavia, come altre EBPM, enoxaparina deve essere sospeso per ventiquattro ore prima di procedure invasive, in particolare rachicentesi.
Dosi
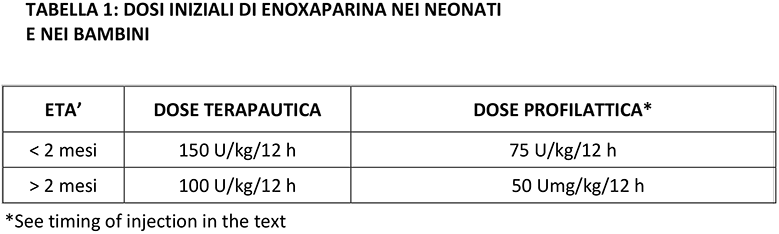
La tabella 1 riassume le dosi di enoxaparina più comunemente utilizzate.
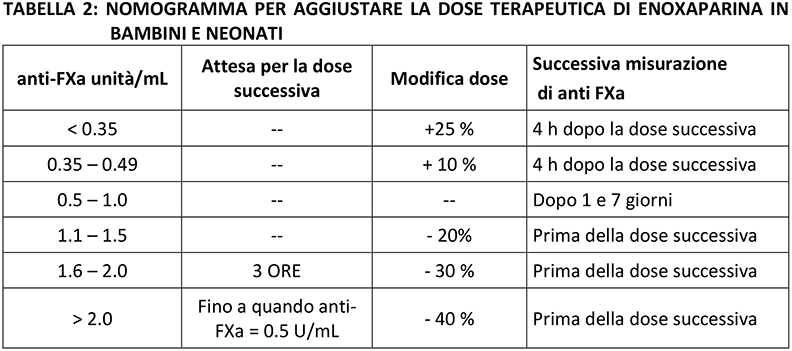
La tabella 2 mostra il nomogramma per aggiustamento della dose.
Vale la pena ricordare che alcuni report suggeriscono dosi iniziali più elevate per i neonati, soprattutto se prematuri: 1,7 mg / kg due volte al giorno per i bambini nati a termine e 2,0 mg / kg due volte al giorno per i neonati prematuri; tuttavia, la sicurezza e l’efficacia di quest’approccio non sono state confermate da studi clinici. Nella nostra esperienza, le dosi consigliate su Chest e sopra riportate erano coerenti con il livello di anti-FXa quando misurato, nella maggior parte dei pazienti, anche se per alcuni neonati si è giunti a dosi più alti come già descritte.
Monitoraggio
Il trattamento con Enoxaparina è monitorato misurando l’inibizione del FXa (antiFXa) in campioni prelevati da quattro a sei ore dopo la somministrazione sottocutanea e raccolto in 3,2% di citrato. Mentre il monitoraggio non è di solito necessario nel bambino, può essere utile nei neonati che in genere richiedono dosi più elevate e che prendono rapidamente peso in solo un paio di settimane. In questo setting, il monitoraggio può inizialmente essere effettuato ogni due settimane, in particolare nei pazienti trattati con dosi terapeutiche. Il range terapeutico è 0,5-1 unità anti-FXa / mL. I medici dovrebbero verificare con il proprio laboratorio la compatibilità tra i sistemi diagnostici e il farmaco, perché sono disponibili reagenti differenti, e alcuni di essi hanno bisogno di curve dedicate per ogni tipo di eparina.
Frequenza di somministrazione
Il dolore e il disagio generati dalle iniezioni devono essere presi in considerazione quando si prescrive un trattamento con enoxaparina in bambini e neonati. Il trattamento della trombosi acuta deve essere iniziato con due iniezioni giornaliere che possono generare problemi di compliance. Come già scritto, si può suggerire che quando l’accettazione del trattamento è un problema, un programma di singola somministrazione giornaliera potrebbe essere efficace per la profilassi secondaria assicurando un’attenta misurazione di anti-FXa dopo ventiquattro ore.
Durata del trattamento
In generale, le EBPM dovrebbero essere utilizzate per i primi 5-10 giorni di trattamento del TEV in bambini e adulti, con successiva embricazione con gli antagonisti della vitamina K. Solo bambini Alcuni suggeriscono di prendere in considerazione un trattamento per un anno o più, quando non si ottiene la ricanalizzazione, in presenza di trombofilia ad alto rischio (livello del FVIII maggiore di 150 U/dL, D-Dimero superiore a 500 ng/mL, almeno tre trait trombofilici e anticorpi antifosfolipidi persistenti) o in presenza di sindrome post trombotica. Infine, la terapia anticoagulante a tempo indeterminato è indicata per bambini con recidive di TEV secondaria ad anomalie strutturali venose. Per i trattamenti a lungo termine, iniezioni sottocutanee ripetute possono essere molto impegnative sia per i bambini sia per i genitori e la terapia anticoagulante per più di tre mesi è di solito eseguita con AVK.
Migliorare la compliance
Un dispositivo sottocutaneo che è stato inizialmente creato per la somministrazione di insulina può essere uno strumento utile in questo scenario (Insuflon®). È un piccolo dispositivo con minimo ”spazio morto” (0,0075 mL) che è inserito per via sottocutanea e può essere lasciata in situ per una settimana riducendo così il dolore e disagio delle iniezioni. Si rende il trattamento più fattibile per i genitori che devono somministrare il farmaco e che di solito preferiscono utilizzare questo strumento, piuttosto che per iniettare il loro bambino ogni giorno. L’Insuflon deve essere usato con cautela soprattutto in neonati di peso molto basso. Un’altra possibilità è di applicare un anestetico topico che però può compromettere l’assorbimento del farmaco.
Il programma due volte al giorno è molto impegnativo per i pazienti pediatrici, e spesso i genitori chiedono una riduzione di un’iniezione ogni ventiquattro ore. Quando uno schema di monosomministrazione quotidiana è adottato per superare significativi problemi di compliance, è necessario monitorar e i livelli di anti-FXa post ventiquattro ore. Infine, enoxaparina può essere somministrato per via endovenosa se un catetere venoso centrale è disponibile.
Tuttavia, mentre questa via di somministrazione è efficace nell’evitare il disagio delle iniezioni, altera fortemente la farmacocinetica del farmaco: i livelli anti-FXa hanno mostrato un picco 1-2 ore dopo l’iniezione, e in rapida diminuzione entro 6-8 ore. Pertanto sarebbero teoricamente necessarie tre iniezioni endovenose che rendono a tale programma raramente fattibile e limitato ai portatori di linee venose.
Gestione di mini-dosi
La dose di enoxaparina è calcolata sul peso del paziente, e quello dei bambini varia notevolmente. Così, i bambini più piccoli richiedono minime quantità del composto. Per la maggior parte dei farmaci confezionati per gli adulti la somministrazione a bambini e neonati è soggetta a errori di diluizione.
La siringa preriempita di enoxaparina sodica a minore dosaggio contiene 2000 UI in 0,2ml. Nei neonati e nei bambini, è comune dovere somministrare mini dosi come 100-300 U (0,01-0,03 mL). 0.01 mL è uguale a un’unità della siringa da insulina. Per tali piccole quantità, lo spazio morto di siringhe, aghi e Insuflon®, il già citato dispositivo sottocutaneo, potrebbe rappresentare un problema. Sebbene siringhe insulina senza spazi morti siano disponibili in commercio, le comuni siringhe da insulina hanno 0,05 mL di spazio morto, che può fortemente influenzare la quantità finalmente iniettata. Così il primo consiglio è di utilizzare siringhe insulina senza spazio morto.
Questa soluzione presenta comunque qualche debolezza. Infatti, anche se 200 UI (0.02 mL) potrebbero essere teoricamente presa dalla siringa preriempita o dal flacone originale, poiché corrispondono a due unità sulla siringa da insulina, la quantità iniettata infine potrebbe risentire lo spazio morto dell’Insuflon®. (tabella 3a). In questo caso una diluizione del farmaco è utile per limitare l’effetto dello spazio morto.
Nella tabella 3b riassumiamo come diluire il contenuto della siringa da 20 mg-2000 UI / 0,2 mL per preparare mini-dosi con siringhe insulina. In breve, dosi superiori a 1000 UI potrebbero essere facilmente presi dalla siringa UI 2000 utilizzando siringhe senza spazio morto, e non è necessaria alcuna diluizione. Con siringhe senza spazio morto, la diluizione del contenuto della siringa di enoxaparina da 20 mg-2000 UI / 0,2 ml in 1 ml H20 o soluzione glucosata al 5% è utile quando si devono somministrare dosi inferiori a 1000 UI attraverso Insuflon®. Infine, la stessa diluizione è sempre consigliata per dosi inferiori a 500 UI. Nelle tabelle 3a e 3 b si evidenzia l’effetto dello spazio morto dell’Insuflon® sulla quantità effettivamente iniettata di farmaco. È evidente che quando la dose programmata è inferiore a 600 UI (6 mg) senza diluizione, la quantità di farmaco che non è iniettata è più del 15% della dose programmata.


Bibliografia
Molinari AC, Banov L, Bertamino M, Barabino P, Lassandro G, Giordano P. A Practical Approach to the Use of Low Molecular Weight Heparins in VTE Treatment and Prophylaxis in Children and Newborns. Pediatr.Hematol.Oncol. 2015 Feb;32(1):1-10.







